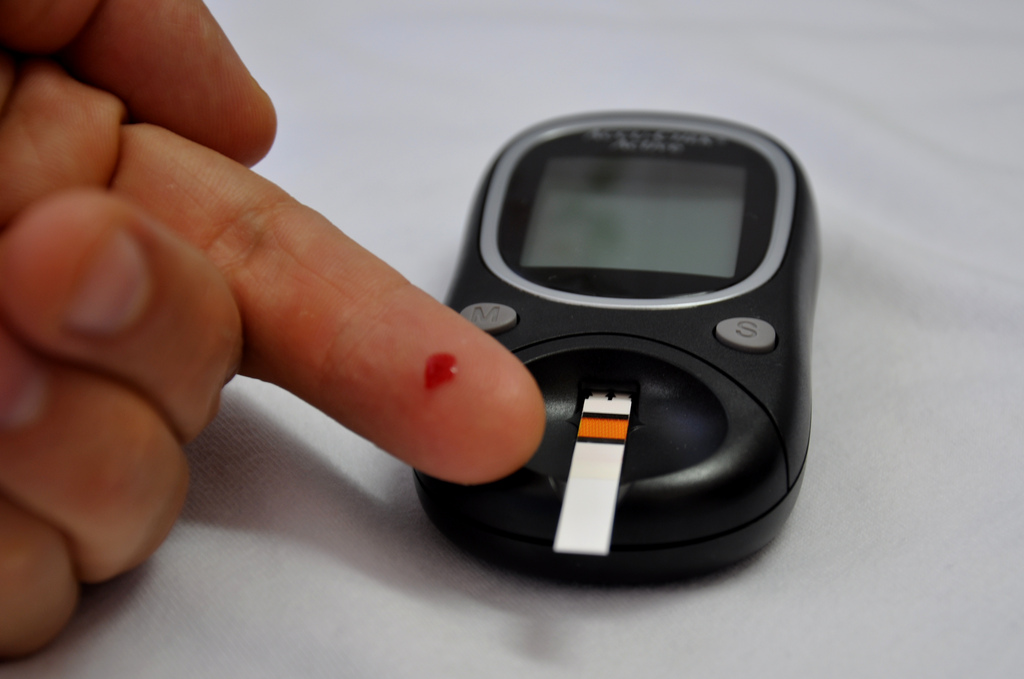
Insulina Made in Italy
- Elisa Scaringi
- 19 Febbraio 2016
- Salute & Medicina
- 0 Comments
Buone notizie per i pazienti diabetici. Approda anche in Italia, dopo il via libero europeo, la prima insulina biosimilare. Si tratta di una versione equivalente rispetto al “farmaco originatore”, con analoga efficacia clinica e caratteristiche fisico-chimiche similare, che faciliterà non soltanto la cura del diabete, di tipo 1 e 2, ma consentirà anche al Servizio Sanitario Nazionale di spendere molto meno. L’insulina biosimilare, infatti, costerà circa il 25% in meno rispetto a quella “originator”.
Si tratta di una versione “simile”, ma non “uguale”, rispetto al farmaco già utilizzato in ambito clinico (chiamato “originatore”), per il quale sia scaduta la copertura brevettuale. Il biosimilare non è però un farmaco generico: se quest’ultimo, infatti, è la “copia esatta” di un farmaco di sintesi chimica, il biosimilare, invece, è una semplice “riproduzione”, data da un processo produttivo biotecnologico che presenta un certo grado di variabilità.
Secondo il rapporto 2015 “Arno Diabete”, elaborato dalla Società Italiana di Diabetologia e dal Consorzio Interuniversitario Cineca, l’incidenza della patologia sulla popolazione italiana sarebbe stimata intorno al 6,2% (circa 3.780.000 italiani affetti da diabete). La proiezione sale a 5 milioni di malati, con un’incidenza dell’8,1%, se si aggiungono i casi di diabete non diagnosticato (1 italiano ogni 4 pazienti noti). “Il Servizio Sanitario Nazionale deve porsi dunque il problema della riduzione dei costi”, rileva il presidente dell’Associazione Medici Diabetologi, Antonio Ceriello. “La nuova possibilità di utilizzare farmaci altrettanto efficaci, ma meno costosi, è, oggi, una svolta”.
La nuova molecola, prima del suo genere a essere stata approvata in ambito europeo, ha inoltre il pregio di essere un farmaco Made in Italy. Nato infatti dall’alleanza di due importanti aziende farmaceutiche come la tedesca Boehringer Ingelheim e la Eli Lilly, verrà prodotto nel sito di Sesto Fiorentino (Firenze) della Lilly.
“Va detto innanzitutto che stiamo parlando di un biosimilare, non di un farmaco generico”, spiega Giorgio Sesti, professore ordinario di medicina interna all’Università di Catanzaro. “Si tratta cioè di un prodotto complesso, realizzato grazie a tecniche di biologia molecolare a immagine e somiglianza del farmaco biologico originatore. Può essere leggermente diverso perché la variabilità nella produzione di molecole biologiche complesse è maggiore, ma in clinica deve poi avere caratteristiche di efficacia e sicurezza simili all’originale, senza differenze statisticamente significative. Le procedure per la registrazione di un biosimilare sono infatti tutt’altro che semplificate, come accade invece per i generici per i quali è necessario un solo studio di bioequivalenza: un biosimilare deve sottostare a regole stringenti per la produzione, deve superare una mole importante di studi preclinici e deve ripercorrere l’iter dei trial clinici che ne certificano l’assoluta sovrapponibilità di comportamento rispetto all’originator”.
L’insulina biosimilare potrà inoltre essere utilizzata attraverso un dispositivo iniettivo di nuova generazione: una penna pre-riempita, di cui saranno disponibili anche cartucce per le tipologie ricaricabili. Questo per consentire anche ai circa 800mila pazienti di tipo 2, non insulino-dipendenti, di poter passare al trattamento iniettivo: in molti casi, infatti, accorgimenti quali dieta, esercizio fisico e farmaci orali non sono sufficienti a tenere sotto controllo la glicemia.
“L’insulina, nonostante sia un trattamento fisiologico che ripristina una funzione ormonale deficitaria, è vista da questi pazienti come una sorta di “ultima spiaggia”, un segno di malattia a uno stadio terminale”, continua il professore Giorgio Sesti. “C’è perciò una barriera psicologica rilevante da parte del malato, cui si aggiunge la riluttanza di molti medici: la gestione di una terapia insulinica richiede maggiori colloqui, più attenzione, più tempo da dedicare all’educazione del paziente per insegnare come modificare i dosaggi in base alla glicemia, ai pasti consumati o all’attività fisica svolta. Così, spesso passano anche quattro o cinque anni prima che un paziente per cui sia indicata l’insulina cominci davvero la cura. L’insulina glargine biosimilare, grazie ad un device più semplice e accurato e a nuovi strumenti educazionali e servizi sviluppati, può rendere l’inizio della terapia basale più facile”.
Elisa Scarlingi




